On porte à 350°C quatre ballons de 1L:A,B,C et Drenfermant chacun 0,50 mmol de H2. Les ballons sont maintenus à cette température durant des durées différentes,puis ils sont brutalement refroidis. Le diiode restant dans chaque ballon est d'abord dissous dans une solution d'iodure de potassium(qui prend une couleur jaune),puis il est dosé par une solution de thiosulfate de sodium de formule Na2S2O3 et de concentration molaire C=0,050mol.L-1.
- La fin du dosage est indiquée par la décoloration de la solution de diiode.Soit Véq le volume de la solution de thiosulfate de sodium nécessaire pour obtenir la décoloration.On donne les couples rédox suivant:I2/I- 0,62V; S4O62-/S2O32- 0,09V.
- Expliquer le principe général de la manipulation.
- Expliquer le principe du dosage de diiode en solution et écrire l'équation de la réaction correspondante.
- Complèter le tableau suivant regroupant les résultats expérimentaux obtenus:
ballon A B C D t (min) 50 100 150 200 Véq (mL) 16,6 13,7 11,4 9,4 nS2O32- (mmol) n(I2) restant (mmol)
Le diiode constitue l'oxydant fort et l'ion thiosulfate le réducteur fort
I2 + 2 S2O32- donnent 2 I- + S4O62-
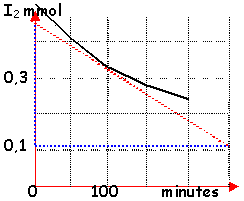 | la vitese de formation de HI est 2 fois plus grande (voir coef. équation) |




0 commentaires:
Enregistrer un commentaire