| Reaction avec les ions iodure et peroxodisulfate | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
A 25°C, une solution contenant des ions peroxodisulfate S2O82- et des ions I- se transforme lentement. Le tableau ci-contre traduit l'évolution d'un systeme contenant initialement 10 mmol de peroxodisulfate d'ammonium et 50 mmol d'iodure de potassium.
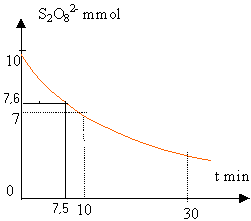 composition du mélange à t=7,5 min: le graphe donne la quantité de matière d'ion peroxodisulfate :voisine de 7,6 mmol faire un tableau d'avancement : à la fin l'un au moins des réactifs a disparu soit 10-xmax=0 ou 50-2xmax=0 xmax=10 mmol et les ions iodures sont en excès. 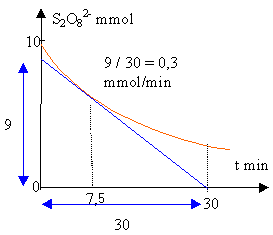 la vitesse de disparition du peroxodisulfate à t=7,5 min est voisine de 0,3 mmol/min en faisant les produits en croix, ontrouve que ces deux vitesses sont égales. le temps de demi réaction est le temps au bout duquel la moitié du réactif limitant a disparu : cela correspond à 5 mmol de peroxodisulfate. lire le temps correspondant sur le graphe : environ 24 min. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Popular Posts
-
Le graphe ci dessous représente l'évolution, en fonction de l'avancement de la réaction x, des quantités de matière des réactifs et ...
-
There was a dead silence instantly, and Alice thought to herself, 'I wonder what they WILL do next! If they had any sense, they'd t...
-
On souhaite préparer une solution aqueuse d'hydroxyde de sodium , de concentration c b =0,10 mol/L, à partir d'une solution S 1, de...
-
Reaction avec les ions iodure et peroxodisulfate A 25°C, une solution contenant des ions peroxodisulfate S 2 O 8 2- et des ions I - se t...
-
On mélange dans un bécher 100 cm 3 d’une solution de concentration molaire 2.10 -2 mol.L -1 d’iodure de potassium KI et 100 cm 3 d’une s...
-
On étudie la transformation lente de réduction des ions peroxodisulfate S 2 O 8 2- (aq) par les ions iodure I - (aq). Ces deux réactifs ap...
-
Sommaire Planification Etudes urbaines Etude centre-bourg Périmètre de Protection Modifié Cahier de...
-
Jabas - Library
Labels
- 1. Cours de chimie
- 1. Cours de physique
- 1. Devoirs de contrôle
- 1. Devoirs de synthèse
- 1. Séries d'exercices
- 2. Cours de chimie
- 2. Cours de physique
- 2. Devoirs de contrôle
- 2. Devoirs de synthèse
- 2. Séries d'exercices
- 3. Cours de chimie
- 3. Cours de physique
- 3. Devoirs de contrôle
- 3. Devoirs de synthèse
- 3. Séries d'exercices
- 4. Cours de chimie
- 4. Cours de physique
- 4. Devoirs de contrôle
- 4. Devoirs de synthèse
- 4. Exercices corrigés
- 4. Séries d'exercices
- City
- Computer
- Cuisines
- Destination
- Fashion
- Foods
- Gallery
- Libellé 1
- Libellé 2
- Music
- People
- Phones
- Photography
- rss
- Server
- Speaker
- Tablets
- Tech
- Travel
- Trends
- Video
- Wedding
- World News




0 commentaires:
Enregistrer un commentaire